期待のアビガンが簡単に処方できない理由:専門家のイロメガネ(1/5 ページ)
新型コロナウイルスの感染者数が急増している現在、「アビガン」という薬が特効薬として期待されている。しかし、アビガンは他のインフルエンザ薬が無効、または効果が不十分な新型もしくは再興型のインフルエンザが発生した場合で、なおかつ国が承認した場合のみ使える薬だ。アビガンの「催奇形性(さいきけいせい)」というリスクががその理由の一つだ。
新型コロナウイルスの感染者数が急増している現在、「アビガン」という薬が特効薬として期待されている。先日、アビガンの治験が日米で開始されたと報じられたばかりだが、安倍首相は4月7日の記者会見でそのアビガンに触れ、現在の備蓄量の3倍、200万人分を準備すると話す熱の入れようだ。
筆者は薬剤師の資格を持ち、製薬会社を顧客とする医薬品開発の会社に10年以上勤めてきた。医薬品の開発や治験に関しても詳しい。そんな立場から、現在話題になっているアビガンや、アビガンを取り巻く状況、そしてその問題点について説明したい。
新薬ができるまで
「アビガンの治験」が始まったと書いたが、治験とはなにか? そもそも薬はどのように作られるのか? どうやって新薬ができるのか?
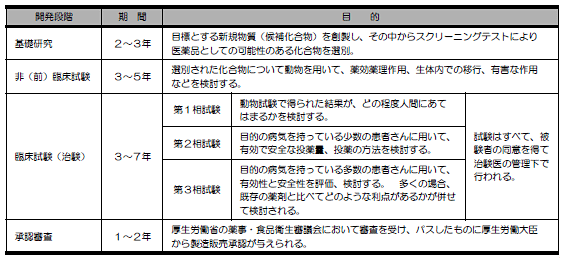
薬の開発は、薬になりそうな化合物を探し出す「基礎研究」からスタートする。次にラットなどの動物を使って、その化合物が安全で効果があるかどうかを調べる「非臨床研究」へと進む。その後、人を使って調べることになるが、これを「治験」という。
治験はまず少人数の健康な人を対象に行い、次は少人数の患者に行う。効果が出そうであれば、さらに人数を増やして試験を行う。このように、3つの段階がある(第1相から第3相)。もちろん十分に説明を受けたうえで、本人の同意が必要だ。
この中で、薬を患者に投与して、血液検査を始めとするさまざまなデータを収集する。そのデータを解析して、ようやく本当に効果があるといえるかが分かる。効果ありという結果が出たら、国に承認申請する。
その結果、承認が得られれば、めでたく「医薬品」として販売でき、病院で処方ができるようになる。
その後も「製造販売後調査」が行われ、安全かどうか、有効な薬かどうかが確かめられる。最終段階として「再審査」と呼ばれる審査があり、場合によっては承認取り消し、効能効果の削除または修正が行われることもある。
薬は、「何に効くか」「何に使うか」がきちんと定められている。これを「適応」という。アビガンは既にインフルエンザ薬として承認を受けているが、新型コロナウイルスへの適応はまだ承認されていない。そのため「適応追加」を目的として、第2相もしくは第3相試験の治験から行われる。
アビガンの新型コロナウイルスに対する治験は、どんなやり方で実施しているかはまだ公表されていない。しかし、既に中国では2本の治験が行われて、その結果、新型コロナウイルスにファビピラビル(アビガンの一般名称)が有効であるとの結果が出ている。
しかし、この中国での論文は取り下げとなった。理由は現時点では不明であるが、近日中に差し替え版が掲載され、取り下げた理由も記載されるようだ。
Copyright © ITmedia, Inc. All Rights Reserved.
関連記事
 コロナウィルスで打撃を被るのは「製薬会社」となり得る意外なワケ
コロナウィルスで打撃を被るのは「製薬会社」となり得る意外なワケ
不謹慎だと思われる方もいるかもしれないが、株式市場では、早速「コロナウィルス関連株」の物色が始まっている。特に、今後需要が見込まれるマスクや医療廃棄物を手がける会社の株価は、ここ2週間で大きく増加した。 AIが予測する、コロナショックで増益する企業、減益する企業
AIが予測する、コロナショックで増益する企業、減益する企業
テキストマイニングを用いてAIで企業や経済の先行きを分析するxenodata lab.(東京都渋谷区)は、新型コロナウイルスの国内上場企業への影響予測を公開した。それによると、世界的に感染が拡大した際の影響は、各業界共通で部品サプライヤーへの減益影響が大きいと予測された。 円安・株安はなぜ起きた? 日本はもはや「スタグフレーション入り」したのか
円安・株安はなぜ起きた? 日本はもはや「スタグフレーション入り」したのか
「円安になると株価は上がる――」。この法則がいまや崩れようとしている。景気が後退しているにも関わらず物価が上昇する状態を、スタグフレーションという。通常、景気が悪い中で物価が上がる場面は限定的であるが、今回においては消費税の増税による半ば強制的な物価の押上げが、これを現実のものにするかもしれない。 コロナ相場で要注意? 老舗企業に潜む「隠れ不動産会社」の見つけ方
コロナ相場で要注意? 老舗企業に潜む「隠れ不動産会社」の見つけ方
国内の不動産投資信託の状況を示す、東証REIT指数が大幅に下落している。そして上場企業の中には、“隠れ”不動産銘柄とも呼ぶべき企業が存在していることをご存知だろうか。 コロナ・ショックからの回復を支える財政拡大
コロナ・ショックからの回復を支える財政拡大
過去最大級の経済対策を決定した日本では、今後感染拡大防止が奏功した段階で、地域活性化などのアイデアの具体化を含む追加対策が打ち出されることになるだろう。米国では、追加の経済対策が議論され始め、欧州でもEUがルールを一時緩和し、機動的な財政政策が打てるようになった。