iPS医療製品、年内にも実用化 アムシェプリ開発の住友ファーマが挑むコスト回収の壁
世界初の人工多能性幹細胞(iPS細胞)由来の再生医療等製品「アムシェプリ」が、5月20日から公的医療保険の対象となる。山中伸弥京都大教授が2006年にマウスのiPS細胞作製を報告して約20年。アムシェプリの製造販売は条件・期限付きで認められた「仮免許」の段階にあり、販売開始後は、期限内に有効性を示すデータを収集し開発コストを回収できるかが焦点になる。
「ようやくここまできた。喜んではいるが、身を引き締めている」
アムシェプリを開発した住友ファーマ(大阪市)の木村徹社長は13日の26年3月期決算説明会でこう述べた。
20日から保険適用
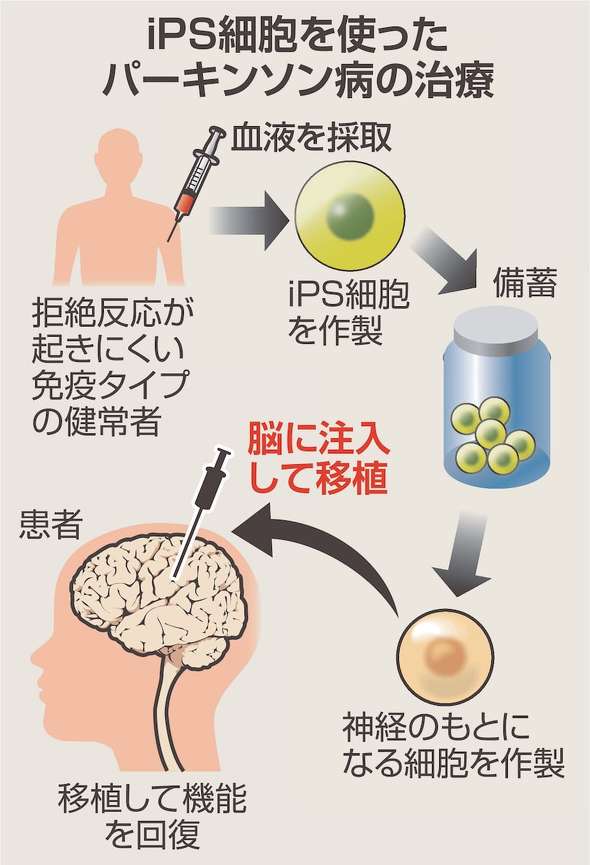
パーキンソン病を対象としたアムシェプリは、3月に条件・期限付き承認を取得し、厚生労働相の諮問機関、中央社会保険医療協議会(中医協)が20日からの保険適用を了承した。薬価は5530万6737円。
生きた細胞を扱う再生医療等製品は品質管理が難しく、有効性を示す十分なデータを得るまでに時間がかかる。条件・期限付き承認制度は、有効性を推定できる段階で製造販売を認め、患者に早期にアクセスする仕組みだ。事業者側は期限内に有効性と安全性を裏付けるだけの症例を収集し、再審査で本承認されれば製造販売を継続できる。ただ有効性確認のハードルは高く、これまで本承認に至った例はない。
アムシェプリの承認期限は33年までの7年間。住友ファーマによると今秋ごろに販売を開始し、26年中に治療を始める予定。7施設で18〜65歳の患者計30人に臨床試験(治験)を実施し、その後65歳超の患者5人にも移植する。治験終了後に対象施設や患者を順次拡大する方針。木村氏は「有効性、安全性をよりしっかり示していく」と強調した。
「利益出すのは責務」
再生医療等製品は開発コストを反映し、価格は高額になりやすい。ただ条件・期限付き承認は有効性が推定される段階であり、有用性加算などの上乗せ分を適用するかは本承認の際に判断する。
木村氏は保険適用を歓迎する一方、「現状のコスト構造からすると明らかに赤字だ。もう少し高い薬価をお願いしていたので、少し残念」と語った。「目標値が決まれば利益が出る形に仕上げていく。われわれの得意とするところであり、責務でもある」と述べた。
立命館大の間宮弘晃准教授(医療経済学)は、アムシェプリの保険適用について「価格交渉がまとまらず適用に至らない製品もある中で、第1ステップをクリアしたといえる」と指摘。「事業者側は、条件に合致する患者を集めて症例を積み上げ、責任をもって結果を出すことが求められる」と語った。(清水更沙、清宮真一)
類似品なく原価計算方式
iPS細胞を使った再生医療等製品「アムシェプリ」の公的医療保険適用が決まった。
──Q:患者1人当たりの価格は5530万6737円。どのように決まったのか
A:条件・期限付き承認を受けた再生医療等製品の価格は、類似の効果がある医薬品と比較する方式が原則。類似品がない場合に原価計算方式を採用する。iPS細胞由来のアムシェプリは類似品がないとして、後者の方式で算定された。
──Q:患者負担はどうなるか
A:保険適用で原則3割になる。医療費が高額になれば高額療養費制度の対象となり、年収や年齢に応じた支払額となる。8月に新たに年間の上限額が設けられ、年収約370万〜770万円の場合だと、自己負担は53万円となる。
──Q:どのような患者が対象になるか
A:既存の治療薬では効果が得られていない患者が対象で、当面は限定的となる。治療施設も、高度な移植を行い、副作用などに迅速に対応できる大学付属病院など要件が定められている。
関連リンク
copyright (c) Sankei Digital All rights reserved.
Special
PR