ITmedia NEWS >
企業・業界動向 >
新型コロナ、5分で陽性判定の感染検査キット、FDAが緊急使用許可
» 2020年03月30日 08時20分 公開
[佐藤由紀子,ITmedia]
米医療企業Abbottは3月27日(現地時間)、新型コロナウイルス感染症の陽性判定を5分で行える同社の検査キットが、米食品医薬品局(FDA)から緊急使用許可(emergency use authorization、EUA)を受けたと発表した。
EUAとは、認可された一部の研究所および医療機関でのみでの使用許可。AbbottはEUAの下、米国の医療機関で1日当たり5万件のテストを可能にする目標で検査キットを増産しているという。4月中に約500万件の検査を実施する計画だ。
この検査キットは、同社の検査機器「ID NOW」で利用する。ID NOWの検査機器自体は2014年に発売したもので、インフルエンザやRSVの検査で全米の多数の医療機関で使用されている。
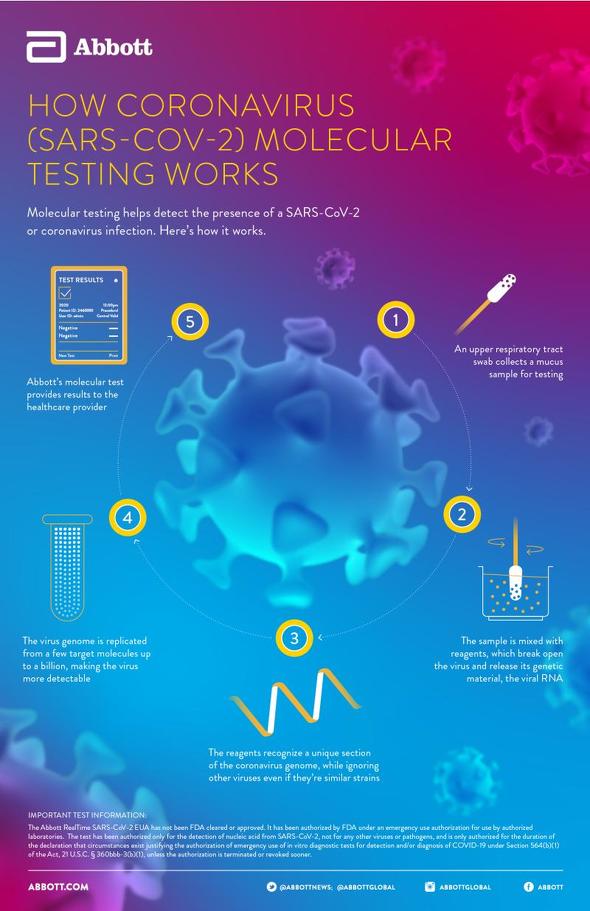
Abbottの検査では、ウイルスのゲノムの微少なセクションを識別し、検出可能になるよう増幅するプロセスを採用。これにより、従来数日かかった検査結果が、陽性の場合は5分、陰性の場合は13分で判定できるとしている。
同社は政府当局と協力し、検査数を拡大していくとしている。
関連記事
 新型コロナ感染を15分で判定、クラボウが検査キット発売 少量の血液で検査可能
新型コロナ感染を15分で判定、クラボウが検査キット発売 少量の血液で検査可能
クラボウが、新型コロナウイルスの抗体を15分で検出できる検査試薬キットを発売する。日本国内の研究・検査機関向けで、価格は税別2万5000円。 新型コロナウイルス Googleの闘い方
新型コロナウイルス Googleの闘い方
新型コロナウイルスのパンデミック宣言から約2週間。Google(とその系列)によるさまざまな取り組みをご紹介。伝統のエイプリルフールは来年にお預けに。 AWS、新型コロナ診断法開発支援で2000万ドル(約22億円)のイニシアチブ立ち上げ
AWS、新型コロナ診断法開発支援で2000万ドル(約22億円)のイニシアチブ立ち上げ
Amazon.com傘下のAWSが、新型コロナウイルスの診断ソリューション開発支援に2000万ドルを投じ、イニシアチブを立ち上げた。24時間以内に診断可能なシステムを目指す。参加者はAWSのインフラだけでなく、専門家の支援も受けられる。
関連リンク
Copyright © ITmedia, Inc. All Rights Reserved.
Special
PRアイティメディアからのお知らせ
SpecialPR
あなたにおすすめの記事PR