性能5倍の「蓄電池」、自動車変えるリザーバ型:蓄電・発電機器(4/5 ページ)
金属硫化物電極の反応機構を解明
カチオンが移動するリザーバ型蓄電池にはハロゲン化物を用いるもの以外に、硫化物を用いるものがある。図3で「M-S」と示したタイプだ。以下のような反応で充放電する。
4Li +アモルファスTiS4 ↔ Li4TiS4
これまでLiS系はサイクル寿命が非常に短かったのだという(図5左)。これは放電時に正極材料の硫黄が電解液に溶け出してしまうためだ。
そこで金属(上の反応式ではチタン)と共有結合するような方策を講じた。安定した充放電が可能になり、おそらくチタンと硫黄がアモルファス構造を採っていると予測できたが、確認する手段がない(性能を改善する糸口がない)。
「アモルファス構造では、短い周期構造がないため、通常のX線回折では観察できなかった。そこで、大型放射光施設Spring-8の高エネルギー回折を用いて、長い範囲の秩序構造の情報を得た。放電が終わったLi4TiS4と充電が完了したTiS4の電極の全体像を比較することにより、図5左の下に示した状態を採ることを確認できた」(同氏)。
多電子移動が可能なハロゲン化蓄電池
3つ目の開発成果は、アニオンが移動するリザーバ型蓄電池に関するもの。高いエネルギー密度を狙っているものの、リチウムは登場しない。
図6に示したように負極に金属ハロゲン化物、正極に別の金属を置く。両極間を移動するのはハロゲンのイオンだ。例えば、フッ化物イオン(F−)を用いたときは、次のような反応で充放電する。ランタン(La)の価数が3つ、銅(Cu)の価数が2つ変化しており、効率よく電子を扱うことができる。多電子移動が可能であるため、エネルギー密度の高い蓄電池として期待できそうだ。
2LaF3 + 3Cu ↔ 2La + 3CuF2
Copyright © ITmedia, Inc. All Rights Reserved.
人気記事トップ10
- 日本ペロブスカイト太陽電池普及促進協議会が発足 規格統一など共通課題に対応
- 中東情勢の影響と今後の見通しは? 燃料・石油製品の供給力確保と国内資源開発の現況
- ペロブスカイト/CIGSのタンデム型太陽電池 世界最高の効率25.14%を達成
- 非FITモデルで400カ所の太陽光発電所を新設 中部電力と丸紅新電力
- 未精製の水素と燃料電池で発電 富士電機と東亞合成が共同実証
- 生成AIでダム管理業務の暗黙知を見える化 東京電力が実証実験
- ソフトバンクがバッテリー製造事業を開始 2028年度にGWh規模の量産体制へ
- 第3回長期脱炭素電源オークションの結果が公表 落札は32件・730万kWに
- 積水化学がフィルム型ペロブスカイト太陽電池を販売開始 まずは金属屋根向けに
- 核となる“水素大動脈構想”とは? 水素・アンモニアの社会実装とロードマップ案
最新プレスリリース
- 地域の風力発電所を活用したふるさと納税の返礼品「御前崎市産CO2フリーでんき」の提供を開始
- 内航船革新的運航効率化・非化石エネルギー転換推進事業の2次公募開始〜内航海運における省エネルギー化・非化石エネルギー転換を支援します〜
- 音声基盤クラウドサービス「BellCloud+?/BellCloud+CX?」に、KCS準拠の高品質ナレッジ自動生成ソリューション「Knowledge Generator」を連携し、通話録音データの活用領域を拡大
- 揚水発電機を用いた随意契約の締結に伴う需給調整市場の週間市場商品における募集量の見直しについて [東京電力パワーグリッド株式会社]
- 【5月25日受付開始!】令和8年度徳島県地域脱炭素移行・再エネ推進事業補助金(ZEH+補助事業/個人向け太陽光発電設備・蓄電池補助事業)
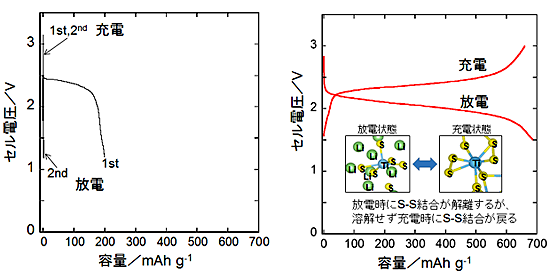 図5 硫黄電極の充放電挙動 左:2回目の充放電で既に容量が0近くまで落ちている。右:アモルファス構造を採る金属硫化物電極の充放電の挙動と、微視的な構造。出典:NEDO、京都大学
図5 硫黄電極の充放電挙動 左:2回目の充放電で既に容量が0近くまで落ちている。右:アモルファス構造を採る金属硫化物電極の充放電の挙動と、微視的な構造。出典:NEDO、京都大学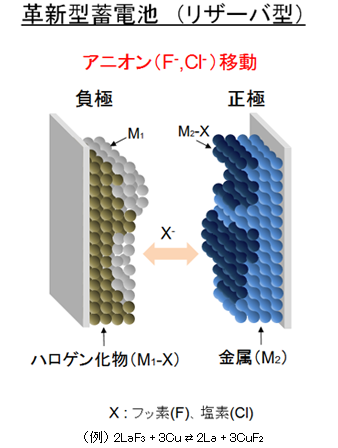 図6 アニオンが移動するリザーバ型蓄電池 フッ化物イオンや塩化物イオンが電荷を運ぶ。出典:NEDO、京都大学
図6 アニオンが移動するリザーバ型蓄電池 フッ化物イオンや塩化物イオンが電荷を運ぶ。出典:NEDO、京都大学


